2020年12月15日,欧盟发布新规(EU) 2020/2081和(EU) 2020/2096,修订了REACH法规的附录XVII。其中(EU) 2020/2081新增REACH附录XVII中第75项条目。(EU) 2020/2096修订REACH法规附录XVII限制篇中的第3、28-30、43、46项,删除已经纳入欧盟POPs法规管控的第22、67和68项,法规在官方公报发布后的第二十天(2021年1月4日)生效。
一、新增附录XVII的第75项条目
2022年1月4日之后,纹身用途的混合物如不符合下述至少一条特定的限制要求,则不得用于纹身,投放欧盟市场。限制物质和要求主要包括:
A、法规(EC) No 1272/2008附件VI第3部分中归类为1A、1B或2类致癌物或1A、1B或2类生殖细胞致畸物的物质,在混合物中的浓度≥0.00005%(按质量计);
B、法规(EC) No 1272/2008附件VI第3部分中归类为1A、1B或2类生殖毒性的物质,在混合物中的浓度≥0.001%(按质量计);
C、法规(EC) No 1272/2008附件VI第3部分中归类为1、1A或1B类皮肤刺激物的物质,在混合物中的浓度≥0.001%(按质量计);
D、法规(EC) No 1272/2008附件VI第3部分中归类为1、1A、1B或1C类皮肤腐蚀性物质或2类皮肤刺激物,或1类严重眼睛损伤或2类眼睛刺激物的物质:(i)如果该物质仅用作pH调节剂,其浓度≥0.1%(按质量计);(ii)在其他情况下,其浓度≥0.01%(按质量计);
E、法规(EC) No 1223/2009附件II中所列物质,在混合物中的浓度≥0.00005%(按质量计);
F、法规(EC) No 1223/2009附件IV中g列(产品类型、身体部位)规定的物质在如下用途的混合物中的浓度≥0.00005%(按质量计):(i) “冲洗产品”; (ii) “不得用于粘膜用产品”; (iii) “不得用于眼用产品”;
G、法规(EC) No 1223/2009附件IV的表格中的h列(即用制剂中的最大浓度)或i列(其他)所列物质不符合该列所规定的条件;
H、于本附件(REACH附录XVII)附件13中所列的物质,在混合物中的浓度等于或大于附录中对该物质规定的浓度限值。(具体可查询附录XVII附件13)
此外法规还规定了特定的豁免物质、供应商在投放市场前应在混合物上标注相关信息、以及特定物质的浓度信息等内容,具体参见原文文件,在此不做详述。
二、修订第3、28-30项条目
删除第3项限制要求中对R65的引用,并修改了第3段和第5段的内容。删除第6、7段。
第28-30项条目,修改了与之相关的附录1、附录2、附录3、附录4、附录5和附录6的标题,在附录2、附录5和附录6中新增了相关的具体物质的名称及编号,并新增f点关于(EU) 2017/745涵盖产品的豁免,其中欧盟法规(EU) 2017/45为关于医疗器械的法规,详见法规原文。
三、删除第46项条目的CAS号和EC号,并删除第22、67和68项条目
删除了第46项中壬基酚的CAS号和EC号,以明确法规管控所有类别的壬基酚类物质。
第22项五氯苯酚及其盐和酯,第67项十溴二苯醚,第68项PFOA及其盐和相关物质(2020年7月4日已生效),已经纳入到欧盟POPs法规的管控,此三项从REACH法规限制篇中删除。
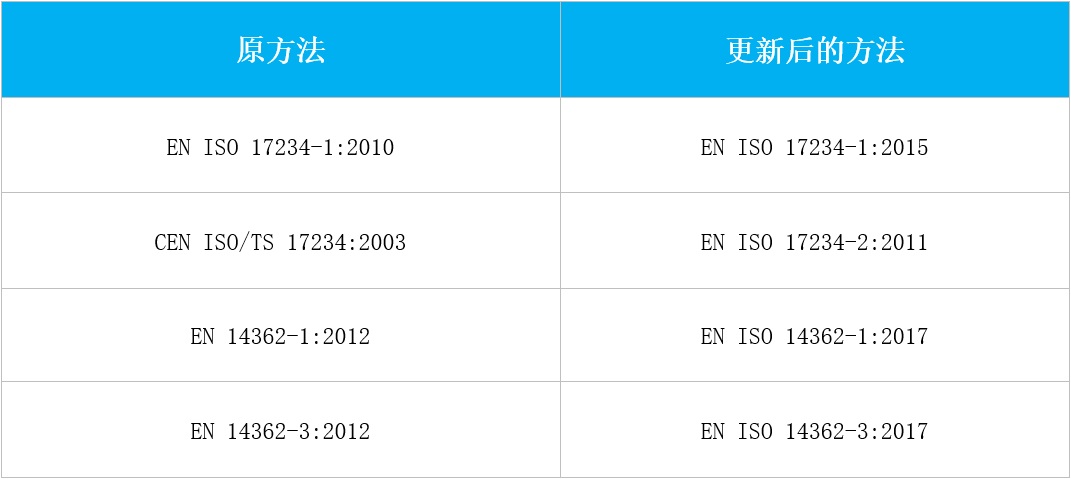
四、更新第43项中附件10的测试方法
以上信息摘自欧盟官方公告网:
相关网址:
https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX%3A32020R2081&qid=1609116650404
https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX%3A32020R2096&qid=1609294275379